European Radiology:放射组学用于区分放射性脑损伤和胶质瘤复发的系统回顾及分析
2025-03-06 shaosai MedSci原创 发表于陕西省
影像组学通过从医学图像中提取大量特征并转化为高维数据,能从常规医学图像中捕捉肿瘤的空间异质性,揭示非影像组学方法可能遗漏的隐藏信息。
胶质瘤是中枢神经系统肿瘤的一大类,世界卫生组织(WHO)将其分为 1 至 4 级。高级别胶质瘤(3 级和 4 级)通常为恶性,复发率和死亡率高;低级别胶质瘤(1 级和 2 级)侵袭性相对较低,但仍有复发风险。高级别胶质瘤术后标准治疗包括放疗和替莫唑胺化疗,这些治疗手段也可单独或联合用于低级别胶质瘤。然而,这种治疗策略常导致放射性脑损伤,如假性进展和放射性坏死。放射性脑损伤形式的治疗相关效应可能意味着治疗有效,仅需对症处理而非调整治疗方案;相反,肿瘤复发通常需要更积极的抗癌治疗和可能的再次手术。因此,及时准确地检测肿瘤复发对优化临床治疗方案至关重要。
在诊断影像上区分放射性脑损伤和实际肿瘤复发颇具挑战。根据神经肿瘤反应评估威廉亚洲博彩公司 ,MRI 是评估治疗后肿瘤反应的推荐标准诊断方法。然而,这两种情况在 MRI 上通常都表现为强化病灶,增加了区分难度。先进的成像技术,尤其是灌注 MRI,有望解决这一难题。在灌注 MRI 技术中,动态磁敏感对比(DSC)磁共振灌注在区分胶质瘤复发和放射性改变方面显示出更优的诊断性能。尽管结果令人期待,但成像参数和阈值的差异仍需进一步研究和标准化。FDG - PET 和 FET - PET 在区分这两种情况上也有一定潜力,但由于研究有限且扫描方案存在差异,其疗效尚未达成共识。
在这种情况下,影像组学通过从医学图像中提取大量特征并转化为高维数据,可能提供诊断解决方案。这种方法能从常规医学图像中捕捉肿瘤的空间异质性,揭示非影像组学方法可能遗漏的隐藏信息。结合机器学习算法,影像组学可为肿瘤诊断、分期和预后提供有价值的预测信息,辅助临床决策。然而,由于该技术复杂且多方面缺乏标准化,影像组学研究的方法学质量受到质疑,主要通过影像组学质量评分(RQS)进行评估。最近,如影像组学方法学评分(METRICS)等新工具出现,通过关注研究质量的不同方面,对方法学严谨性进行更细致的评估。

最近,发表在European Radiology 上的一篇文章系统的评价了胶质瘤影像组学中区分放射性脑损伤和肿瘤复发的相关文献。
研究在 PubMed 和 Web of Science 上检索文献(截止日期:2024 年 5 月 7 日)。用影像组学方法学评分(METRICS)和影像组学质量评分(RQS)评估合格论文的质量,分析质量评分工具的可靠性,并进行荟萃分析、meta 回归和亚组分析。
最终27 篇论文纳入定性评估。三位评估者的平均 METRICS 评分和 RQS 百分比评分分别为 57%(标准差 14%)和 16%(标准差 12%)。METRICS 评分的评分者间一致性从差到优不等,而 RQS 显示出中度到优的一致性。两种工具的条目一致性均为中度。对 11 项合格研究的荟萃分析得出受试者工作特征曲线下面积估计值为 0.832(95% 置信区间 0.757 - 0.908),存在显著异质性(I² = 91%),无统计学意义的发表偏倚(p = 0.051)。Meta 回归未确定异质性的潜在来源。亚组分析显示所有亚组均存在高度异质性,在经过适当验证且质量评分较高的研究中 I² 最低,为 68%。除异质性最低的亚组(p = 0.044)外,统计学发表偏倚通常不显著。然而,定性分析(26/27;96%)和主要荟萃分析(10/11;91%)中的大多数研究都报告了影像组学的积极作用,表明存在高度的非统计学发表偏倚。
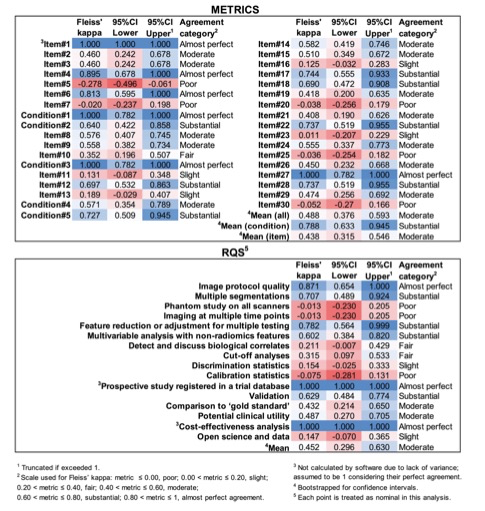
图 基于三个读者评价的项目可靠度分析
本项研究表明,虽然影像组学表现良好,但由于本研究中深入考察的异质性、发表偏倚和质量问题,对结果的解读应谨慎。
原文出处:
Radiomics for differentiating radiation-induced brain injury from recurrence in gliomas: systematic review, meta-analysis, and methodological quality evaluation using METRICS and RQS.Burak Kocak,Ismail Mese,Ece Ates Kus,et al.DOI:10.1007/s00330-025-11401-x
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言




















#胶质瘤# #放射组学#
36 举报