AI辅助罕见病诊断新突破:胶原蛋白VI肌营养不良的深度解析
2025-07-07 熊佳仪 MedSci原创 发表于上海
在罕见病胶原蛋白VI相关先天性肌营养不良症(COL6-CMD)的诊断中,运用人工智能(AI)技术,实现了高准确率的自动图像分类,显著提升诊断效率与客观性。
罕见病因发病率低、临床表现高度异质,且大多遗传性背景复杂,患者往往经历数年漫长诊断过程,延误治疗时机,影响生存质量。近年来,AI技术在医学图像分析领域取得飞跃性进展,尤其在肿瘤学、放射学等领域应用广泛,成功辅助诊断与治疗规划。
然而,罕见病领域AI应用面临训练数据严重不足的瓶颈,限制了深度学习等高复杂度模型的推广。机器学习模型虽对数据量需求较低,也逐步应用于少数罕见病的MRI影像中,但同样数据量限制了模型泛化能力。因而探索适合罕见病特质的数据增广、迁移学习以及多模态融合等策略,成为亟需攻克的重要方向。

COL6-CMD是由COL6A1、COL6A2、COL6A3三基因突变导致胶原蛋白VI结构异常,进而引发肌肉退行性病变。临床上存在从轻度Bethlem肌病(BM)到严重的Ullrich先天性肌营养不良症(UCMD)不同严重度表型。传统诊断依赖临床综合评估、基因检测及组织病理学影像分析,其中共聚焦显微镜能高分辨率观察肌细胞层面胶原纤维网络状态,为细胞层面病理变化鉴别提供关键依据。然而,图像评估过于依赖临床经验且主观性强,难以实现标准化诊断,使得AI辅助技术的应用显得尤为必要。
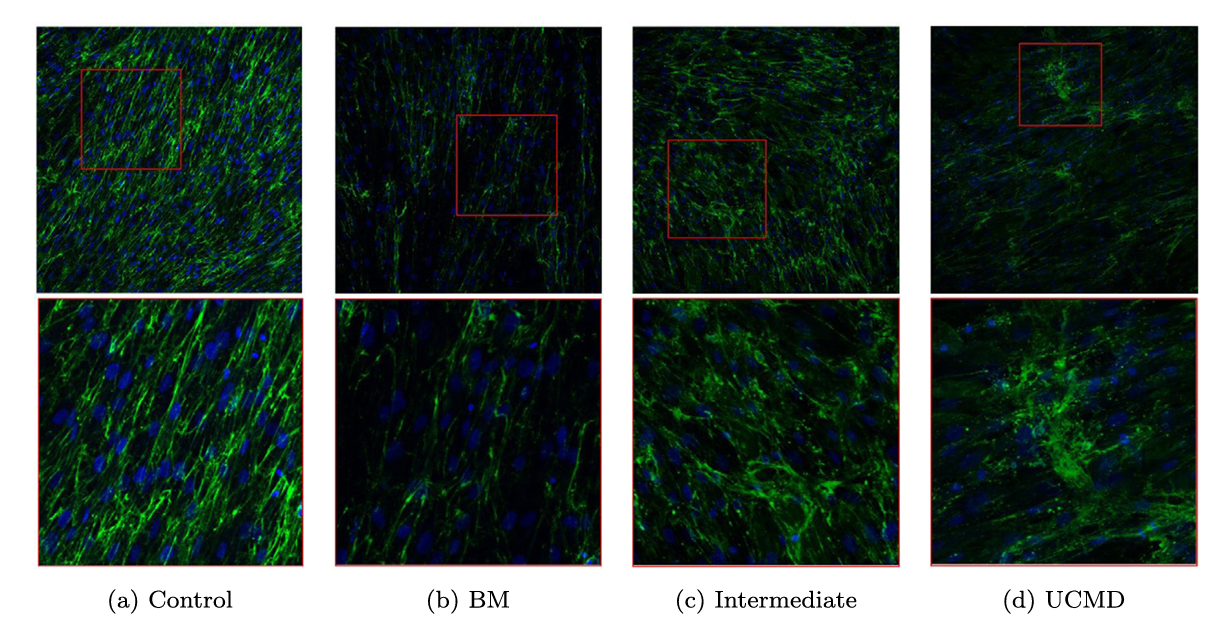
图 1.数据库中存在的对应于皮肤成纤维细胞免疫荧光图像的图像示例
研究方法
本研究使用了由Sant Joan de Déu医院神经肌肉单元和显微成像团队合作采集的数据库,包含16例健康者及16例COL6-CMD患者皮肤活检制备的成纤维细胞共聚焦荧光图像。采用Leica TCS SP8共聚焦显微镜采集,胶原蛋白VI绿荧光、核染色蓝荧光共存,每例制备10个不同采样视野,共计320个三维堆叠图像(160对照、160病理)。
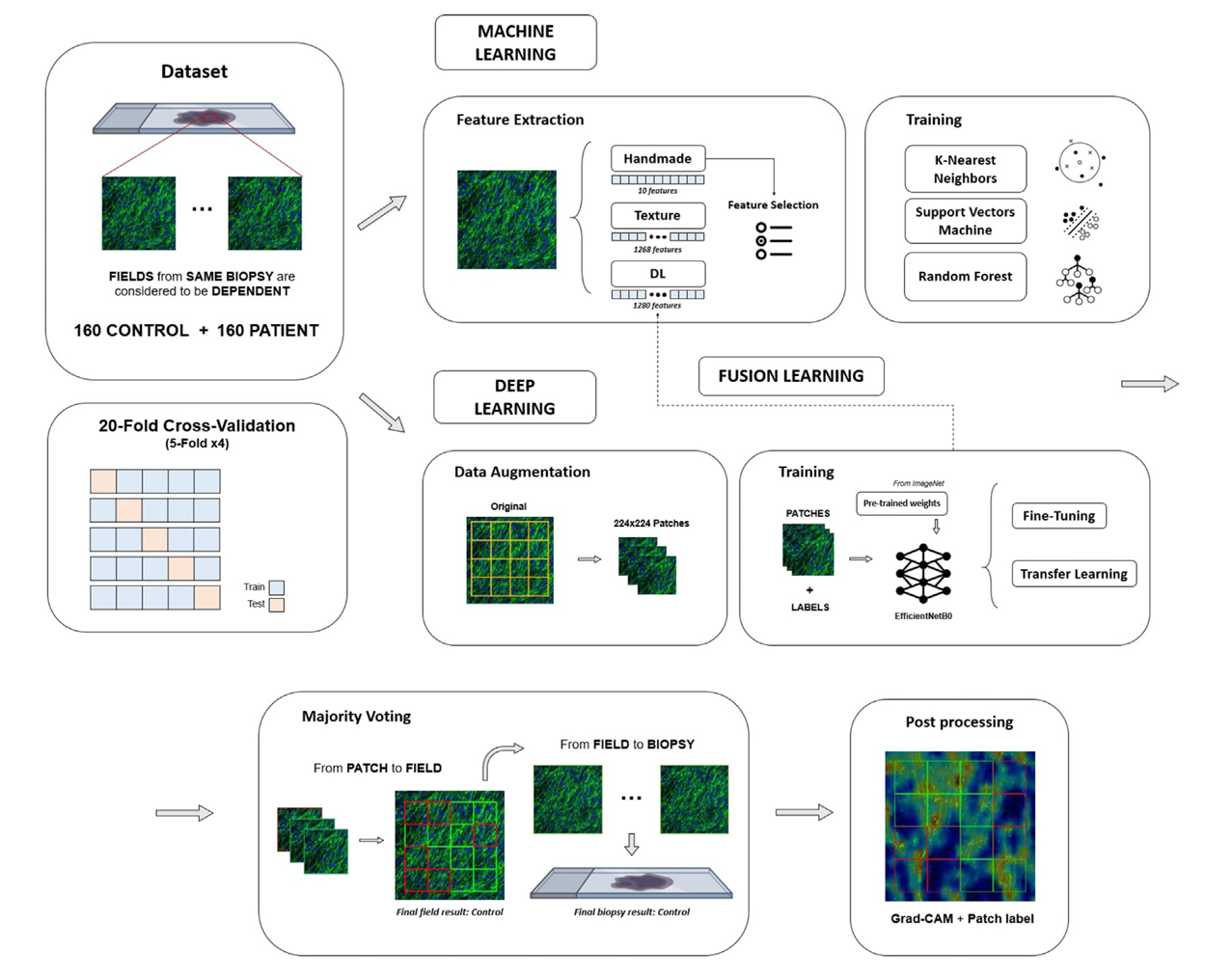
图 2.本研究中对分析流程进行了总结
在AI建模方面:
-
机器学习(ML)方法:提取包括纤维取向、图像信噪比、孔隙率、细胞核形态等10种手工设计特征及局部二值模式(LBP)、梯度方向直方图(HOG)等纹理特征。采用支持向量机(SVM)、随机森林(RF)和加权K近邻(wk-NN)三种分类器进行训练和评估,探索特征选择对性能影响。
-
深度学习(DL)方法:选用预训练的EfficientNetB0架构,采用迁移学习和微调策略,训练时将原始图像分割为224×224像素补丁进行数据增强,考察补丁与原图训练效果差异。
-
融合学习策略:将深度学习模型提取的特征与传统纹理特征结合,转交机器学习分类器,评估融合特征性能改善潜力。
-
模型可解释性:通过Grad-CAM生成热力图,及重建补丁分类结果辅助医师直观理解模型关注的图像区域。
-
交叉验证:采用5折交叉验证,确保不同病例严重度均衡分布,避免样本交叉污染,重复实验20次获得稳健性能估计。
研究结果
- 机器学习表现
采用纹理特征结合SVM分类器效果最佳,AUC高达0.942,显著优于手工特征,显示出特征设计对性能的决定性影响。
- 深度学习表现
迁移学习结合全图训练效果优于微调,AUC达到0.941,且不依赖额外数据增强。
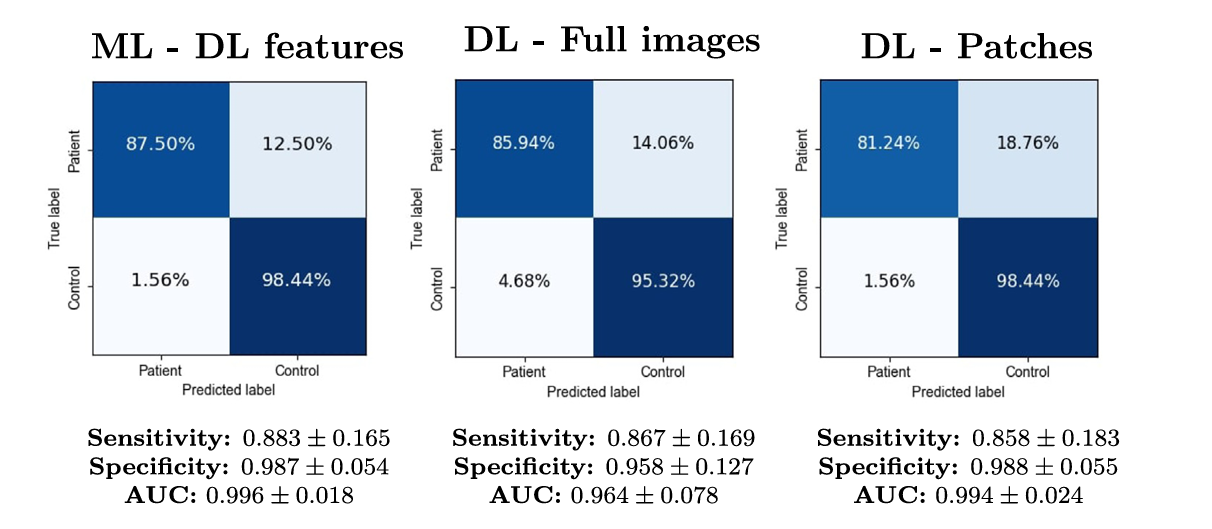
图 3.活检级别的混淆矩阵和指标
- 融合学习
将EfficientNetB0深度特征输入传统ML模型进一步提升性能优势明显,DL特征单独使用时达到最高AUC 0.964,加入纹理特征反而有所降低,表明高维冗余未必有益。
- 病理切片(Biopsy)级别诊断
将多个图像视野结果经多数投票整合,融合策略诊断准确率进一步提升,AUC达到0.996,真正实现临床实用水平。
- 模型可解释性
利用Grad-CAM热力图直观标注模型重点关注区域,与补丁分类结果融合图示清晰可见病变主要特征区,增强模型可信度与临床接受度。
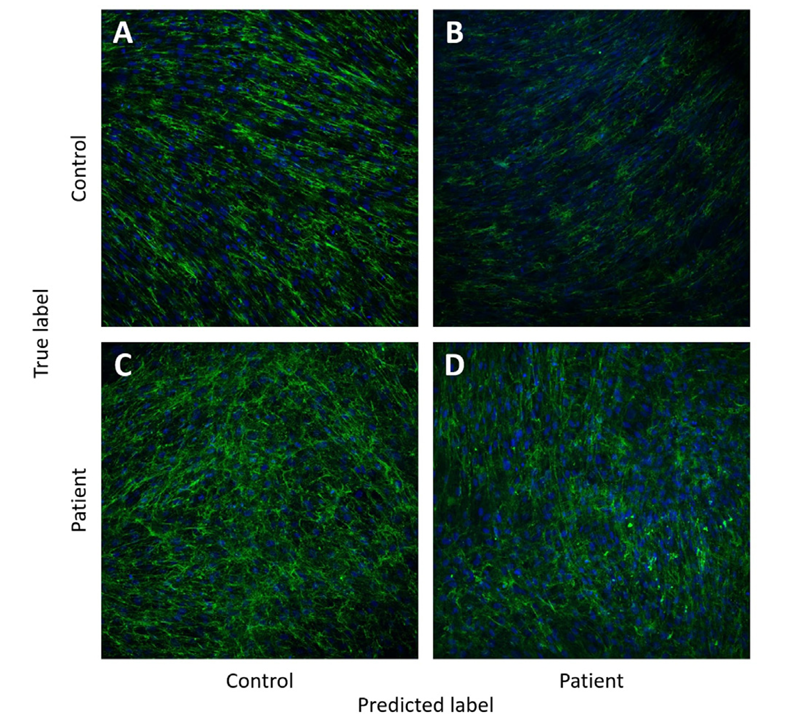
图 4.来自不同主题的四个共聚焦场的示例
研究讨论
本研究系统评估了AI技术在罕见神经肌肉疾病COL6-CMD免疫图像诊断中的适应性。研究表明:
-
罕见病数据稀缺挑战可通过合理划分训练测试集、数据增强(如图像切割补丁)及迁移学习技术有效缓解,避免过拟合,提升泛化能力。
-
ML方法在特征选择和模型智能组合方面仍具优势,尤其手工解释性强,容易为临床接受。但预定义纹理特征对模型性能提升显著,适合跨病种推广。
-
深度学习尤其迁移学习方法更适合复杂非线性特征抽取,融合ML后进一步提升性能,使模型既稳定又灵活匹配真实图像变化。
-
多视野补丁级诊断不仅提升准确率,更方便医生定位重点区域,辅助判断病情严重度及疗效评估。
-
目前模型在极少数样本表现异常表型时仍有误判,提示未来需扩大数据量、引入GAN等生成模型及多中心数据融合,进一步强化鲁棒性。
本研究的成果不仅丰富了罕见肌营养不良症的辅助诊断工具,也为罕见病领域的AI应用提供了科学范式。未来集成多模态数据(临床、遗传、影像)将是精准诊断的关键方向。
williamhill asia 编辑点评
本研究充分发挥了AI在罕见病诊断中的潜力,弥补了传统诊断不足,极大缩短诊断周期,提高了诊断准确率。值得关注的是作者深入比较多种AI策略,并结合罕见病图像自身特征设计了行之有效的数据处理与模型训练流程,极具指导意义。
融合机器学习与深度学习特征的多层次融合策略,有效缓解了数据匮乏带来的瓶颈,为罕见病乃至其他领域提供了可复制范例。此外,模型解释性设计切合临床需求,利于医师对决策机制的理解和信服。
未来,建议作者能够推动数据共享及联合建模,例如利用联邦学习平台提升数据广度,实现多中心模型泛化;多模态结合进一步提升诊疗精准度。同时,利用更多类型的细胞和组织样本进行验证,丰富模型的适用场景,将加速AI驱动罕见病临床转化应用。
原始出处
Computers in Biology and Medicine, Volume 196, 2025, Article 110610, Available online 1 July 2025, https://doi.org/10.1016/j.compbiomed.2025.110610
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言

















AI技术在医学图像分析领域取得飞跃性进展,尤其在肿瘤学、放射学等领域应用广泛,成功辅助诊断与治疗规划。
6 举报
#人工智能# #先天性肌营养不良症#
14 举报