【STTT】新型选择性HDAC I/IIb抑制剂甲磺酸普依司他治疗复发难治性骨髓瘤和淋巴瘤的临床前和I期研究结果
14小时前 聊聊血液 聊聊血液 发表于上海
新型选择性 HDAC I/IIb 抑制剂普依司他,在临床前及 I 期研究中对复发 / 难治性多发性骨髓瘤和淋巴瘤显示出强抗肿瘤活性,尤其淋巴瘤缓解率高,安全性良好。
普依司他
多发性骨髓瘤(MM)和淋巴瘤是全球范围内发病率不断上升的两种血液系统恶性肿瘤。尽管治疗手段有所进步,但MM仍然无法治愈,许多淋巴瘤也会复发和产生耐药性,因此需要开发新的治疗策略。
同时针对关键致病驱动因素和重塑肿瘤微环境是治疗复发或难治性(r/r)多发性骨髓瘤(MM)和淋巴瘤的关键治疗策略。HDAC(组蛋白去乙酰化酶)在肿瘤发生中扮演重要角色,HDAC抑制剂通过维持组蛋白乙酰化状态,促进肿瘤抑制基因和免疫调节基因的转录,从而发挥抗肿瘤作用。新型选择性HDAC I/IIb抑制剂甲磺酸普依司他(purinostat mesylate,PM)拥有一个非线性、大三角形帽和一个刚性连接体,可显著增强其与 I 和 IIb HDAC 的结合亲和力,对 I 和 IIb 的抑制活性和选择性强于所有其他获批的 HDACi,对于淋巴瘤和MM可能有更大获益。
四川大学华西医院牛挺教授、上海交通大学医学院附属瑞金医院赵维莅教授、四川大学华西医院陈俐娟和胡以国教授等共同开展研究,探索了普依司他在MM和淋巴瘤临床前研究及I期研究的疗效、安全性和作用机制,近日发表于《Signal Transduction and Targeted Therapy》。

体外实验: 研究者检测了普依司他对8种MM和8种淋巴瘤细胞系的抗增殖活性,并与泛HDAC抑制剂panobinostat进行比较。结果显示普依司他在所有测试的细胞系中均显示出低于5 nM的IC50值,优于panobinostat。
体内实验: 使用MM1S异种移植小鼠模型、cMYC-KRAS12V原发性浆细胞瘤(PCT)小鼠模型、双表达淋巴瘤PDX小鼠模型、复发难治DLBCL PDX小鼠模型,评估普依司他的体内疗效。普依司他在这些模型中显示出比panobinostat或多药联合治疗方案更好的抗肿瘤活性。
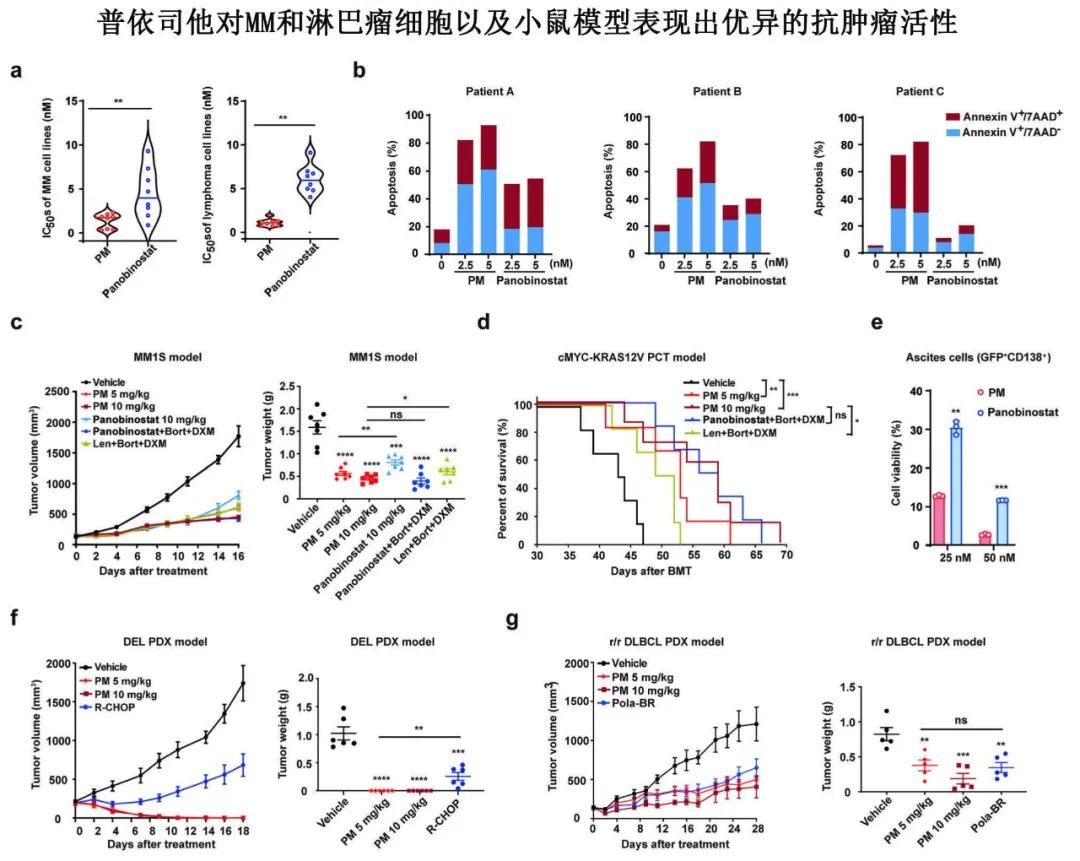
普依司他对MM和淋巴瘤细胞以及小鼠模型表现出优异的抗肿瘤活性
a.人MM细胞系和淋巴瘤细胞系用PM或panobinostat在指定浓度下处理72小时后,分析细胞活性
b.来自MM患者(患者A、B)和淋巴瘤患者(患者C)外周血中的MM和淋巴瘤原代细胞用PM或panobinostat在指定浓度下处理,48小时后分析细胞凋亡。
c.MM1S异种移植模型的肿瘤体积和重量,分别用空白对照、PM、panobinostat、panobinostat+Bort+DXM或Len+Bort+DXM处理。
d.cMYC-KRAS12V诱导的浆细胞瘤(PCT)小鼠从骨髓移植后第35天开始的Kaplan-Meier生存曲线,分别用空白对照、PM、panobinostat+Bort+DXM或Len+Bort+DXM处理。
e.cMYC-KRAS12V小鼠腹水细胞在体外经PM或panobinostat处理后的细胞活性。
f,g.DEL和r/r DLBCL患者来源的异种移植小鼠模型的肿瘤体积和重量,分别用空白对照、PM、R-CHOP方案或Pola-BR处理。
单细胞RNA测序(scRNA-seq): 对5TMM模型小鼠的骨髓细胞进行分析,发现普依司他处理后,单核细胞和T细胞介导的免疫反应增强,表明普依司他通过改善肿瘤免疫微环境发挥抗肿瘤作用。

普依司他治疗后5TMM肿瘤负荷小鼠单核细胞群和基因表达变化的scRNA-seq分析
a.5TMM模型小鼠经空白对照或PM处理后的Kaplan-Meier生存曲线。
b.5TMM模型小鼠经空白对照或PM处理后骨髓中单核细胞的分布。
c.MonoC1、MonoC2和 MonoC10细胞簇的G0富集分析结果。
d、e.对 5TMM模型小鼠经空白对照或PM处理后的MonoC1和Monoc2细胞进行伪时间顺序分析。
f、g.对来自两个独立实验的空白对照和PM处理样本中的“干扰素α反应”和“干扰素B反应”基因集进行伪时间顺序评分。
g.在空白对照组或PM组中指定细胞类型内炎症因子I1-13和I1-19以及趋化因子Cxc110、Cxc112和Cc17的表达水平和频率。
h.与GO富集相关的基因沿伪时间顺序的动态基因表达变化(按层次分为五个基因模块)。
首次人体试验: 在华西医院和贵州医科大学附属医院开展了一项首次人体I期剂量递增的临床试验(NCT05526313),评估普依司他在复发/难治性MM和淋巴瘤患者中的安全性、耐受性和初步疗效,普依司他剂量为1.2-15 mg/m2。在复发/难治性MM患者中,普依司他单药治疗的疾病控制率为72.7%(8/11),客观缓解率为9.1%(1/11)。在复发/难治性淋巴瘤患者中,客观缓解率为61.1%(11/18),其中弥漫大B细胞淋巴瘤(DLBCL)患者中客观缓解率达到63.6%(7/11),包括6例完全缓解。普依司他在1.2-15 mg/m2的剂量范围内显示出良好的耐受性,未观察到剂量限制性毒性(DLT)。主要的治疗相关不良事件为血液学毒性,包括血小板减少(75.9%)、中性粒细胞减少(55.2%)、白细胞减少(41.4%)和淋巴细胞减少(31.0%)。治疗反应者表现出增强的免疫激活,CD3+CD8+ T细胞水平升高,以及干扰素-γ(IFN-γ)和CXCL10等细胞因子水平增加。
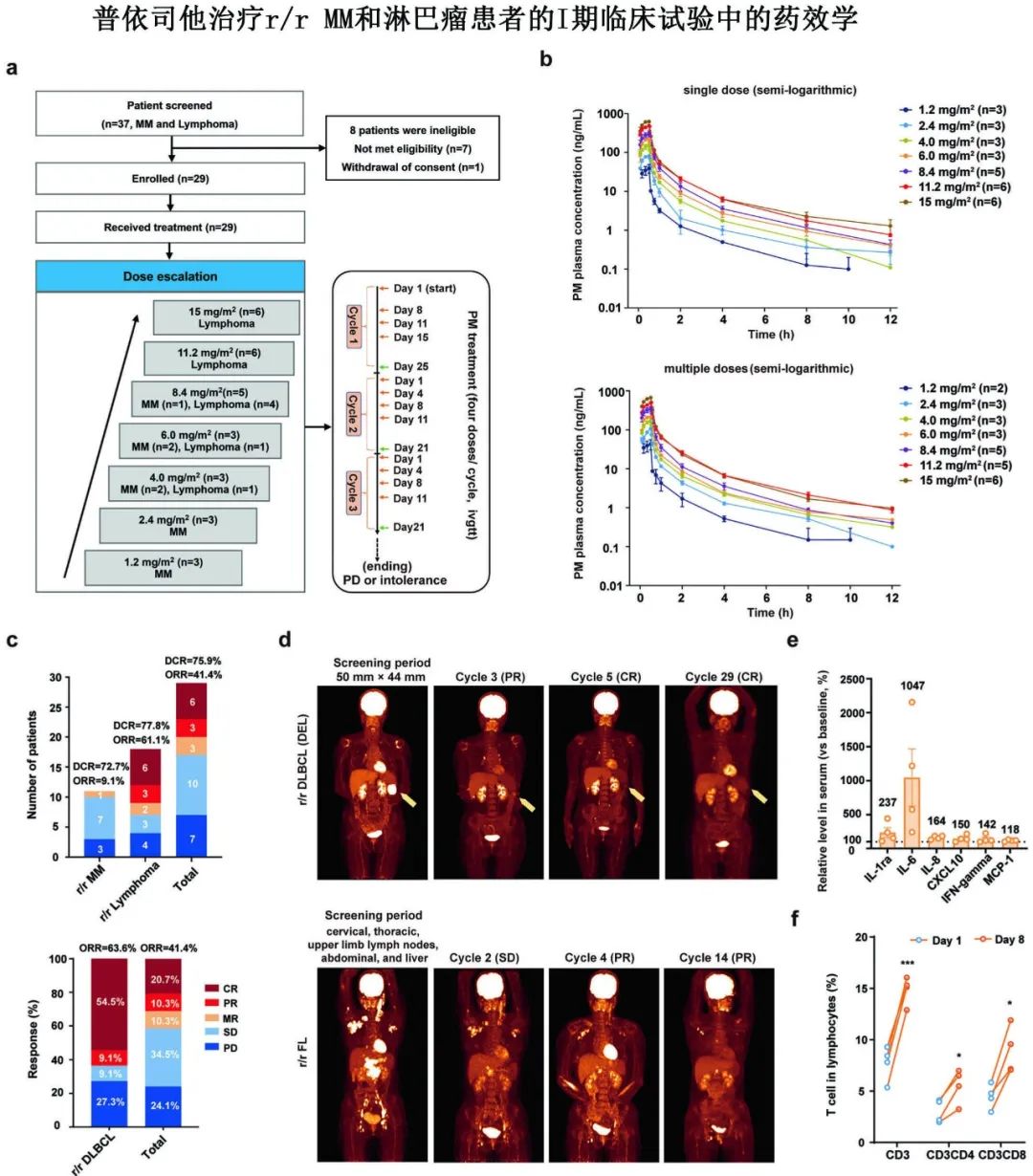
普依司他治疗r/r MM和淋巴瘤患者的I期临床试验中的药效学
a.普依司他治疗r/r MM和淋巴瘤的给药方案示意图。
b.I期患者中的平均血浆浓度-时间半对数曲线
c.I期临床试验的疗效反应。
d.一位r/r DEL DLBCL患者和一位r/r FL患者在筛选阶段以及治疗后不同阶段的PET-CT图像。
e.给药前和给药一周后,r/r MM(n=2)和淋巴瘤(n=2)患者血清中细胞因子水平的变化。
f.给药前和给药一周后,r/r MM(n=2)和淋巴瘤(n=2)患者外周血白细胞中T细胞比例的变化。
总结
普依司他的抗肿瘤活性: 普依司他在体外和体内模型中均显示出比panobinostat更强的抗肿瘤活性,尤其是在抑制肿瘤细胞增殖和诱导细胞凋亡方面。
普依司他的作用机制: 普依司他通过抑制多个对肿瘤生存至关重要的基因表达,并激活免疫相关的信号通路,如干扰素反应和炎症反应,从而增强抗肿瘤免疫反应。
普依司他的初步疗效:普依司他在复发/难治性MM和淋巴瘤患者中显示出良好的耐受性和初步疗效,特别是在淋巴瘤患者中显示出较高的客观缓解率。
普依司他联合治疗的潜力: 普依司他与泊马度胺和地塞米松联合治疗在复发/难治性MM治疗中显示出强大的协同作用,支持进一步进行开放标签、多中心Ib/IIa期临床试验,评估普依司他联合免疫调节剂治疗复发/难治性MM的疗效,以及进行II期单药治疗复发/难治性DLBCL和T细胞淋巴瘤的临床试验。
参考文献
Yang, L., Qiu, Q., Wang, J. et al. Preclinical and first-in-human of purinostat mesylate, a novel selective HDAC I/IIb inhibitor, in relapsed/refractory multiple myeloma and lymphoma. Sig Transduct Target Ther 10, 201 (2025). https://doi-org.ctust.aliya.filescenter.top/10.1038/s41392-025-02285-w
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言















前往app查看评论内容
5 0 举报