弥漫大B细胞淋巴瘤治疗进展:从CAR-T到双特异性抗体的临床选择
2025-07-09 MedSci原创 MedSci原创 发表于上海
2025年最新发表在Journal of Hematology & Oncology杂志的一项综述,全面梳理了原发难治及复发DLBCL患者的治疗策略及未来发展方向。
弥漫大B细胞淋巴瘤(DLBCL)是一种侵袭性强但具可治愈潜力的B细胞肿瘤,标准一线治疗是免疫化疗方案R-CHOP,大约60–70%的患者能获得长期无病生存。尽管如此,仍有30-40%的患者面临复发或难治,治疗挑战巨大。尤其是高危患者,尽管引入了如抗CD79b抗体药物偶联物(polatuzumab-vedotin)联合Pola-R-CHP等新一线方案,但改善有限,原发难治和早期复发患者比例未明显下降。
此外,传统的二线治疗则以含铂化疗为主,随治疗反应不同决定是否进行自体干细胞移植(auto-SCT),而这一策略的治愈率仅约20%,一旦复发预后极差。2017年以后,免疫疗法,尤其是CD19定向CAR-T细胞治疗的兴起,重塑了晚期DLBCL患者的治疗格局。CAR-T在三线及以上疾病显示出约80%的总体有效率及40%以上的长期生存率,最新威廉亚洲博彩公司 已将CAR-T上移至二线,成为早期难治或复发患者的标准选择。
与此同时,双特异性抗体、抗体药物偶联物、小分子靶向药物的陆续获批,丰富了非细胞免疫治疗武器库,为无法接受或复发于CAR-T后的患者提供了更多选项。面对这一复杂多样的治疗阵营,如何科学选择和合理序贯应用成为临床迫切关注的热点。
2025年最新发表在Journal of Hematology & Oncology杂志的一项综述,全面梳理了原发难治及复发DLBCL患者的治疗策略及未来发展方向。该文不仅聚焦新兴细胞疗法和免疫疗法,还整合了真实世界证据和最新临床试验数据,丰富了williamhill asia 对个体化治疗路径的认识,为临床医生提供了宝贵参考。

新获批免疫疗法与靶向药物
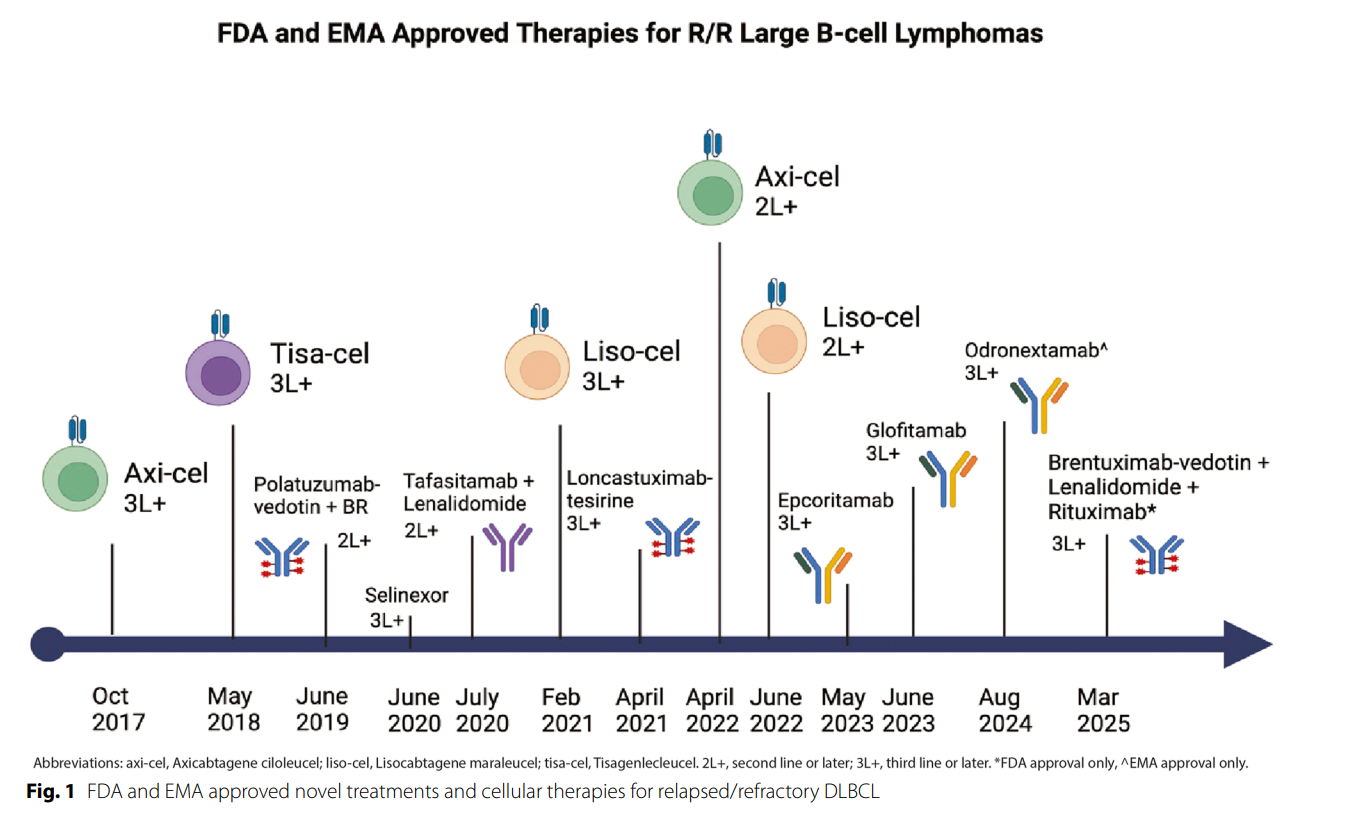
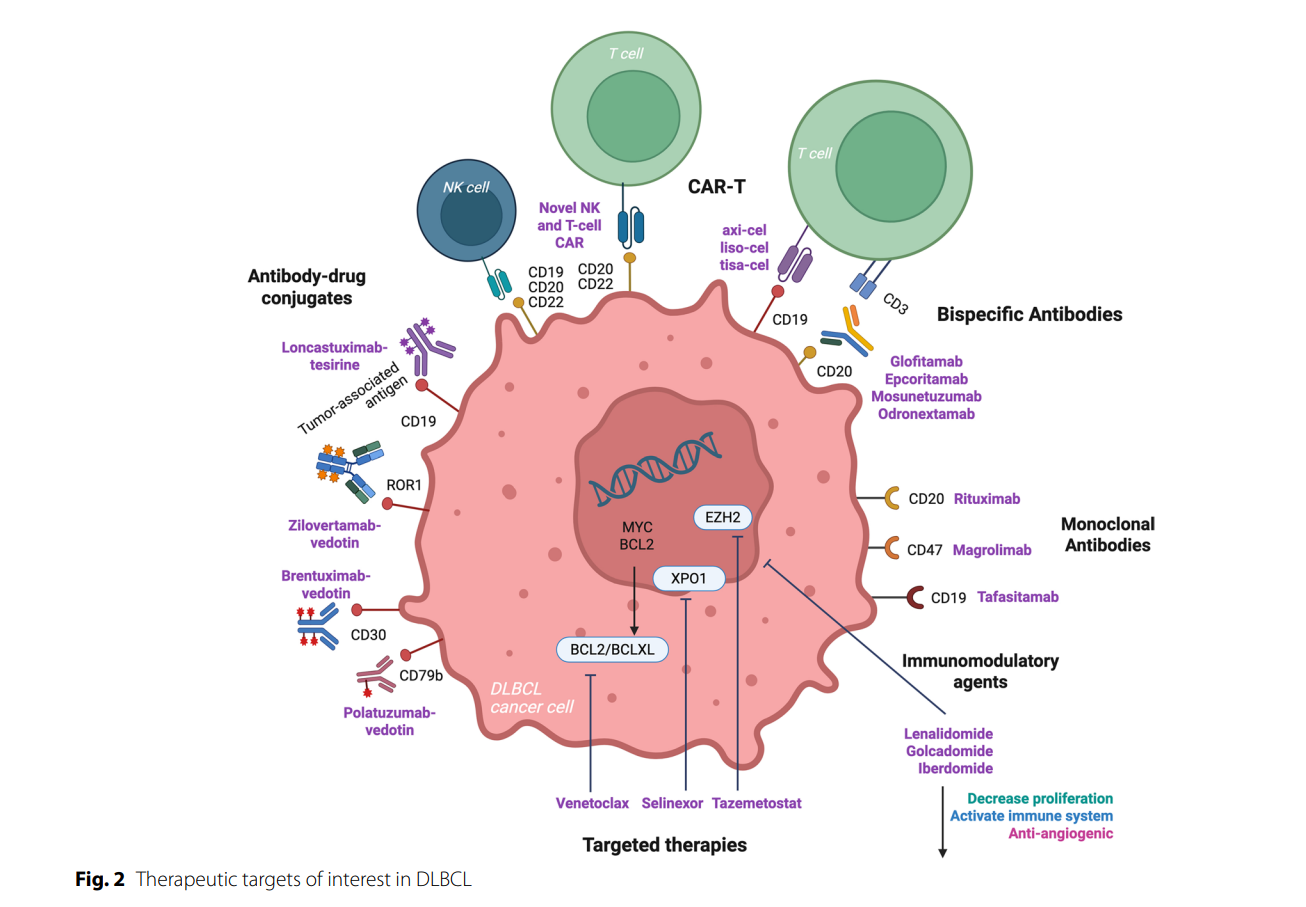
近年来,FDA和EMA批准了多款新药物用于R/R DLBCL,主要分为以下几类:
1,双特异性抗体(BsAbs)——代表药物包括注射方便、起效迅速的Epcoritamab(皮下注射)、Glofitamab(静脉注射)和Odronextamab等,均通过CD20与T细胞CD3双靶点促进肿瘤细胞杀伤。临床数据显示ORR60%左右,CR率约35-40%,部分缓解患者能达到3年以上持续缓解(见表1)。不良反应主要为轻至中度细胞因子释放综合征(CRS)和神经毒性(ICANS),可通过缓释给药和预防性激素辅助控制。真实世界数据提示CD20表达缺失显著降低疗效。
2,抗体药物偶联物(ADCs)——Polatuzumab Vedotin联合Bendamustine+Rituximab(Pola-BR)、Loncastuximab Tesirine(靶CD19)和Brentuximab Vedotin(靶CD30)均显示出不错抗肿瘤活性。Pola-BR最早获批,ORR约56%,CR率达53%。Loncastuximab在LOTIS-2研究中ORR近48%,CR率约25%。新型ADC的优势是靶向性强,降低非特异性毒性,但仍需注意周围神经毒性和骨髓抑制风险。
3,小分子抑制剂——Selinexor作为XPO1抑制剂单药获批,疗效有限,副作用较显著,现临床多关注与其他药物联合应用。此外,新的CELMoD类分子如Iberdomide和Golcadomide也在研发中。
4,非细胞免疫疗法组合——以CD19靶向抗体Tafasitamab联合Lenalidomide组合获批(L-MIND研究),在2-3线患者中ORR57.5%,CR率40%,部分患者达4年以上长期缓解。
CAR-T细胞治疗进展及二线应用
CAR-T细胞治疗历经轴卡替尼西洛乐单抗(axi-cel)、利索卡替尼马洛鲁赛尔(liso-cel)、提沙根乐鲁赛尔(tisa-cel)三大产品的紧密开发,成为复发难治DLBCL的核心治疗手段。
三线及以上CAR-T:ZUMA-1研究中axi-cel表现出82% ORR,58% CR率,长期随访中5年生存率达43%,体现强烈治愈潜力。liso-cel和tisa-cel也显示了类似疗效数据。
二线CAR-T研究:
ZUMA-7(axi-cel)与标准含铂化疗自体移植对比,axi-cel显著改善事件无进展生存(EFS)与总生存(OS),二年EFS分别为41%对16%,4年OS达54.6%对46%。
TRANSFORM(liso-cel)同样展现出优于传统方案的EFS提升,中位EFS 10.1 vs 2.3个月,显著延长生存。
BELINDA(tisa-cel)则未显示出二线优势,治疗效果与标准方案相似。
目前,二线CAR-T以axi-cel和liso-cel成为首选,tisa-cel未获此适应症批准。
CAR-T失败后的治疗挑战
CAR-T治疗失败或复发患者约占50-60%,其预后较差,中位生存仅数月。复发机制复杂,约三分之一病例出现CD19抗原消失,导致CART疗法抗性。
- 复发患者建议活检确认病理及CD19/CD20表达,用于评估后续治疗可行性。
- 双特异性抗体(如epcoritamab、glofitamab)和loncastuximab等ADC在CAR-T失败患者中展现出约50% ORR和35% CR率的活性。
- 结合造血干细胞移植或临床试验探索新一代CAR产品(异源CAR-T、多靶点CAR-T和CAR-NK)为当前突破方向。
未来展望与治疗策略整合
面对递进复杂的治疗选择,临床决策需综合患者年龄、体能状态、合并症、抗肿瘤治疗史、肿瘤生物学特征(包括CD19/CD20表达、细胞起源及分子特征)等因素。精准医疗及分子分型虽尚未全面落地,但液体活检(ctDNA)和早期疗效监测技术的发展,预示着未来可实现动态风险评估和个体化治疗调整。
联合治疗策略如BsAb+ADC、免疫调节剂小分子联合新型免疫治疗多药复合方案(如ViPOR),为难治患者带来新曙光,但耐受性及老年患者用药需谨慎平衡。传统疗法如高剂量化疗+自体/同种异体移植依旧是部分患者疗效保障。放疗作为CAR-T桥接治疗手段正获更多认可,为高风险患者实现疾病控制提供可靠辅助。
原始出处
Bock AM, Epperla N. Therapeutic landscape of primary refractory and relapsed difuse large B-cell lymphoma: Recent advances and emerging therapies. Journal of Hematology & Oncology. 2025;18:68. https://doi.org/10.1186/s13045-025-01702-5
本网站所有内容来源注明为“williamhill asia 医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于williamhill asia 医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“williamhill asia 医学”。其它来源的文章系转载文章,或“williamhill asia 号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与williamhill asia 联系,williamhill asia 将立即进行删除处理。
在此留言











#复发难治大B细胞淋巴瘤#
12 举报